資源簡介
資源簡介
吉林省長春市2025年中考化學模擬試卷1
(考試時間:50分鐘 試卷滿分:50分)
注意事項:
1.答卷前,考生務必將自己的姓名、準考證號填寫在答題卡上。
2.回答選擇題時,選出每小題答案后,用2B鉛筆把答題卡上對應題目的答案標號涂黑。如需改動,用橡皮擦干凈后,再選涂其他答案標號。寫在本試卷上無效。
3.回答填空題時,請將每小題的答案直接填寫在答題卡中對應橫線上。寫在本試卷上無效。
4.回答解答題時,每題必須給出必要的演算過程或推理步驟,畫出必要的圖形(包括輔助線),請將解答過程書寫在答題卡中對應的位置上。寫在本試卷上無效。
5.考試結束后,將本試卷和答題卡一并交回。
可能用到的相對原子質量:H-1 C-12 N-14 O-16 Na-23 S-32
一、選擇題(本大題共10小題,每小題1分,共10分。每小題給出的四個選項中,只有一個選項最符合題目的要求)
1.中華文化源遠流長。下列詞語蘊含化學變化的是( )
A.花香四溢 B.量體裁衣
C.死灰復燃 D.立竿見影
2.2025 年哈爾濱亞洲冬季運動會的吉祥物命名為“濱濱”和“妮妮”,它們佩戴的滑雪鏡鏡片材料為聚碳酸酯塑料,堅固耐用。該塑料屬于( )
A.天然材料 B.合成材料
C.金屬材料 D.復合材料
3.下圖所示是探究鐵銹蝕條件的部分操作,其中正確的是( )
A.取蒸餾水 B.煮沸蒸餾水
C.加入鐵釘 D.吸取植物油
4.下列對物質的用途或實驗事實的解釋中,不正確的是( )
A.冰水共存物屬于純凈物,是因為冰和水都由水分子構成
B.溫度計中的水銀(汞)熱脹冷縮,是因為汞原子的體積發生改變
C.一氧化碳能燃燒而二氧化碳能滅火,是因為兩種物質的分子構成不同
D.稀硫酸和稀鹽酸有許多共同的化學性質,是因為兩種溶液中都含有氫離子
5.化學與人類生活和社會發展關系密切。下列說法錯誤的是( )
A.化學與安全:冬天用煤爐取暖, 應提供充足氧氣
B.化學與環境:用布袋替代塑料袋,可緩解“白色污染”
C.化學與能源:增大煤與空氣的接觸面積有利于煤充分燃燒
D.化學與食品:用福爾馬林浸泡海鮮,延長保質期
6.性質決定用途,下列說法不合理的是( )
A.鹽酸可除鐵銹 B.碳酸鈣可作補鈣劑
C.碳酸氫鈉可治療胃酸過多 D.氫氧化鈉可改良酸性土壤
7.在明代宋應星所著的《天工開物》中,有關火法煉鋅的工藝記載:“每爐甘石十斤,裝載入一泥罐內,然后逐層用煤炭餅墊盛,其底鋪薪,發火煅紅,罐中爐甘石熔化成團。”(注:爐甘石的主要成分是碳酸鋅。)火法煉鋅主要發生的化學反應是:,下列說法不正確的是( )
A.X的化學式是CO B.反應前后固體的質量不變
C.中碳元素的化合價為+4 D.該反應有元素的化合價發生改變
8.圖是鐵元素的“價類圖”及各物質的轉化關系,下列說法正確的是( )
A.a在空氣中燃燒,火星四射生成b
B.d如果是硫酸鹽,其結晶水合物叫作膽礬
C.e是一種亞鐵鹽
D.的制品在潮濕的空氣中會生成
9.歸納推理是學習化學的重要方法,下列有關說法正確的是( )
A.酸雨的pH小于7,則pH小于7的雨水一定是酸雨
B.單質中只含有一種元素,則只含有一種元素的物質一定是單質
C.燃燒都伴有發光、放熱現象,則有發光、放熱現象的變化一定是燃燒
D.化學變化中分子種類發生改變,則分子種類發生改變的變化一定是化學變化
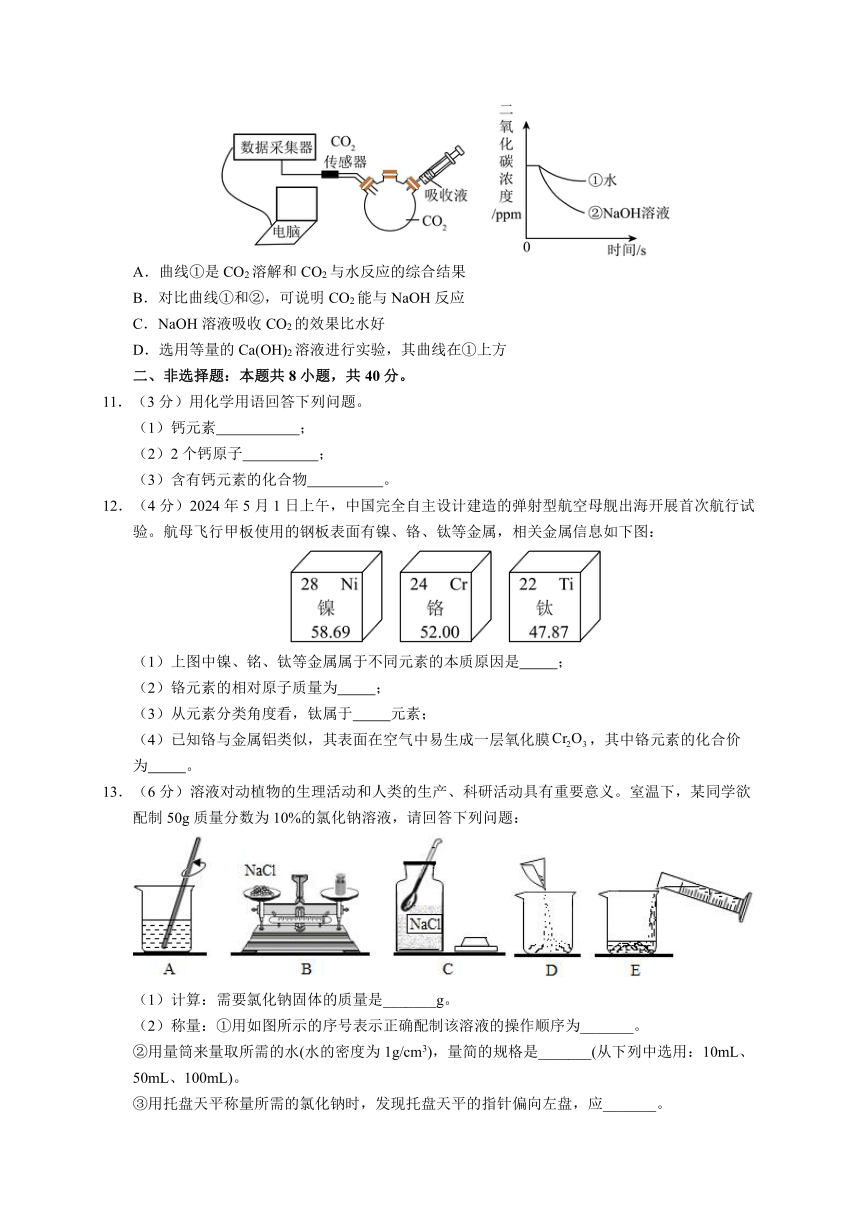
10.實驗小組用傳感器研究等量水、NaOH溶液和Ca(OH)2溶液分別吸收CO2的效果(氫氧化鈣微溶于水,氫氧化鈉易溶于水),實驗裝置及部分測定結果如圖所示。下列說法錯誤的是( )
A.曲線①是CO2溶解和CO2與水反應的綜合結果
B.對比曲線①和②,可說明CO2能與NaOH反應
C.NaOH溶液吸收CO2的效果比水好
D.選用等量的Ca(OH)2溶液進行實驗,其曲線在①上方
非選擇題:本題共8小題,共40分。
11.(3分)用化學用語回答下列問題。
(1)鈣元素 ;
(2)2個鈣原子 ;
(3)含有鈣元素的化合物 。
12.(4分)2024年5月1日上午,中國完全自主設計建造的彈射型航空母艦出海開展首次航行試驗。航母飛行甲板使用的鋼板表面有鎳、鉻、鈦等金屬,相關金屬信息如下圖:
(1)上圖中鎳、銘、鈦等金屬屬于不同元素的本質原因是 ;
(2)鉻元素的相對原子質量為 ;
(3)從元素分類角度看,鈦屬于 元素;
(4)已知鉻與金屬鋁類似,其表面在空氣中易生成一層氧化膜,其中鉻元素的化合價為 。
13.(6分)溶液對動植物的生理活動和人類的生產、科研活動具有重要意義。室溫下,某同學欲配制50g質量分數為10%的氯化鈉溶液,請回答下列問題:
(1)計算:需要氯化鈉固體的質量是_______g。
(2)稱量:①用如圖所示的序號表示正確配制該溶液的操作順序為_______。
②用量筒來量取所需的水(水的密度為1g/cm3),量簡的規格是_______(從下列中選用:10mL、50mL、100mL)。
③用托盤天平稱量所需的氯化鈉時,發現托盤天平的指針偏向左盤,應_______。
A.增加適量氯化鈉固體 B.減少適量氯化鈉固體
C.調節游碼 D.添加砝碼
(3)溶解:將氯化鈉和水依次倒入燒杯中,用玻璃棒攪拌,其目的是_______。
(4)反思:經檢測,所配制氯化鈉溶液的溶質質量分數偏小,其原因可能是_______ 。 (填序號)
①用量筒量取水時,俯視讀數 ②試劑、砝碼的左右位置顛倒且使用游碼
③用量筒量取水時,仰視讀數 ④用于溶解的燒杯中有少量的蒸餾水
⑤轉移溶液時有部分體濺出
14.(4分)水是寶貴的自然資源,回答下列問題。
(1)圖1是電解水實驗簡易裝置圖。通電一段時間后,正極端玻璃管內的氣體是 。
(2)圖2是簡易凈水裝置。該凈水裝置中小卵石、石英砂的作用是 ,該裝置 (填“能”或“不能”)將硬水軟化。
(3)圖3是自來水廠的凈水過程示意圖,其中利用活性炭具有 性,除去水中某些雜質,起到凈水作用。
15.(4分)氣體制備是化學實驗基本技能之一, 某興趣小組利用如圖裝置制取氧氣。
(1)寫出儀器a的名稱 ;
(2)可用過氧化氫溶液和二氧化錳混合制取氧氣。
①選擇的發生裝置為 ;
②將DC 裝置連接并與發生裝置組合后,可收集到干燥的氧氣,則D裝置內盛放的試劑為 ;
(3)實驗室若要制取3.2g氧氣,理論上需要過氧化氫溶液中溶質的質量為 g。
16.(4分)a、b、c三種固體物質的溶解度曲線如圖所示。
(1)P點的含義是 。
(2)t2℃時,等質量a、b、c三種物質的飽和溶液降溫到t1℃,所得溶液中溶劑的質量由大到小的順序是 。
(3)t2℃時,將30g a加入50g水中,充分溶解后,所得溶液的質量是 g。
(4)t2℃時,a、b飽和溶液降溫到t1℃,析出晶體較多的是 。(填“a”或“b”或“無法確定”)
17.(4分)能是綠色的低碳能源。如圖1是“制氫、儲氫、釋氫、用氫”的示意圖。
Ⅰ.“制氫”:通過光伏發電和催化劑的作用,使水分解產生氫氣。
(1)該反應的化學方程式為 。
Ⅱ.“儲氫”:用化學方法將氫氣轉化為甲醇(常溫常壓下液體)。
我國科研人員研制的一種新型催化劑可將二氧化碳和氫氣轉化為甲醇。控制其他條件不變,測定相同時間內不同溫度下甲醇的產率,實驗結果如圖2所示。
(2)分析圖像,可以得出的結論是 。
Ⅲ.“釋氫”:將甲醇轉化為氫氣,通常有以下兩種方案:方案1:CH3OH+H2OCO2↑+3H2↑;方案2:CH3OHCO↑+2H2↑。
(3)對比上述兩種方案,方案1的優點是 (寫一條)。
Ⅳ.“用氫”:氫氧燃料電池能量轉化率高,產物是水,清潔環保。
(4)如果用如圖3表示氫氣燃燒的微觀變化過程,正確的順序為 (填序號)。
18.(11分)堿是化學中一類重要物質,某小組以探究堿的性質為主題開展了以下項目式學習。
(1)氫氧化鈉常溫下是一種白色結晶狀固體,易潮解,極易溶于水,同時 (填“吸收”或”放出”)大量的熱;
(2)取少量氫氧化鈉溶液滴加酚酞溶液,觀察到溶液變紅,說明氫氧化鈉溶液顯 性;
堿與酸能否發生化學反應,化學小組同學開展如下探究。利用圖1裝置探究氫氧化鈉和稀鹽酸反應,用等體積的稀鹽酸和水分別進行實驗,將注射器內液體全部推入,測得一段時間內溫度的變化如圖2所示。
【觀察現象】裝置中溶液由紅色變無色。
【得出結論】
(3)可得到的結論是 。
【分析討論】
(4)100s后鹽酸曲線下降的原因是 。
堿與非金屬氧化物反應,小組同學按照圖3裝置,探究氫氧化鈉溶液與二氧化碳反應的情況,將膠頭滴管中氫氧化鈉溶液注入試管內。
【觀察現象】,U形管內的液面左高右低,液體沿導管流入試管內,且溶液變紅色。
【得出結論】氫氧化鈉溶液與二氧化碳反應。
【分析討論】
(5)有同學認為此實驗現象不能證明氫氧化鈉與二氧化碳發生了反應,原因是 ,還需要完善的實驗。
【查閱資料】氣壓減小時,水的沸點會降低。
【進行實驗】
【觀察現象】
(6)如圖分別進行甲、乙實驗,將5mL濃NaOH溶液、5mL水同時擠壓到對應試管中,振蕩,觀察到 ,證明二氧化碳與氫氧化鈉發生了反應。
(7)二氧化碳與氫氧化鈉溶液的反應無明顯現象;請簡述證明兩者發生反應的方法 。
參考答案
1-10
【答案】C
【答案】B
【答案】B
【答案】B
【答案】D
【答案】D
【答案】B
【答案】C
【答案】D
【答案】D
11.【答案】(1)Ca
(2)2Ca
(3)CaO/CaCO3(合理即可)
12.【答案】(1)質子數不同
(2)52.00/52
(3)金屬
(4)+3
13.【答案】(1)5;
(2)CBDEA;50mL;B;
(3)加速氯化鈉的溶解;
(4)②③④
14.【答案】(1)O2/氧氣
(2)過濾 不能
(3)吸附
15.【答案】(1)酒精燈
(2)B 濃硫酸(濃)
(3)6.8
16.【答案】(1)t ℃時,a、c兩物質的溶解度相等,都是25g
(2)c>b>a
(3)70
(4)無法確定
17.。
【答案】(1)2H2O2H2↑+O2↑
(2)227℃時產率最高或低于227℃時甲醇產率隨溫度升高而升高,高于227℃時甲醇產率隨溫度升高而降低(合理即可)
(3)不產生CO或等質量甲醇可以釋放更多氫氣
(4)bac
18.【答案】(1)放出
(2)堿
(3)稀鹽酸和氫氧化鈉的反應屬于放熱反應
(4)稀鹽酸和氫氧化鈉反應放熱,100s時反應完全,溫度逐漸恢復至室溫
(5)二氧化碳溶于水,也會導致左側試管內的壓強減小,U形管內的液體沿導管流入試管內,氫氧化鈉溶液顯堿性,也能使無色酚酞溶液變紅色
(6)甲中熱水沸騰,乙中熱水未沸騰
(7)向二氧化碳與氫氧化鈉反應后的試管中滴加足量稀鹽酸,若有氣泡產生,證明二者發生反應
PAGE
展開更多......
收起↑
 資源預覽
資源預覽