資源簡(jiǎn)介
資源簡(jiǎn)介
(共15張PPT)
課題3 溶質(zhì)的質(zhì)量分?jǐn)?shù)
學(xué)習(xí)目標(biāo)
1.通過(guò)生活情境了解生活中常見的表示濃度的方法。
2.知道溶質(zhì)質(zhì)量分?jǐn)?shù)可以定量表示溶液的濃度。
3.認(rèn)識(shí)溶質(zhì)質(zhì)量分?jǐn)?shù)的定義及其簡(jiǎn)單的計(jì)算。
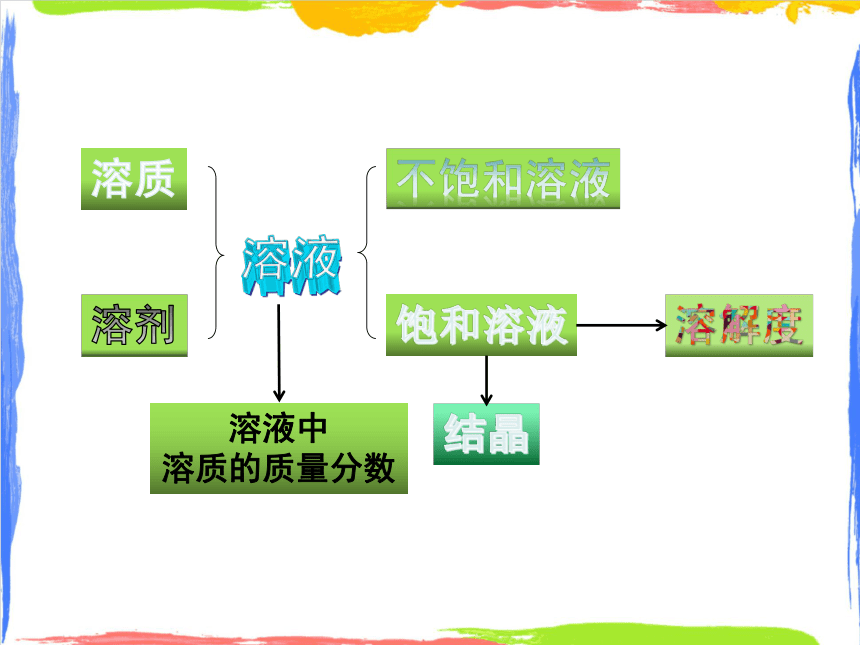
結(jié)晶
溶劑
不飽和溶液
溶質(zhì)
溶液中
溶質(zhì)的質(zhì)量分?jǐn)?shù)
溶液
溶解度
飽和溶液
環(huán)節(jié)一:創(chuàng)設(shè)情境、激發(fā)興趣
情境:小明六歲的弟弟發(fā)燒了,家里備有消毒用的75%的醫(yī)用酒精,奶奶想用它直接來(lái)給小明的弟弟擦身而達(dá)到物理降溫的作用,小明馬上制止了,同學(xué)們,你們能查閱資料了解原因嗎?75%和30%的酒精的區(qū)別是什么嗎?
75%的酒精濃度過(guò)大,發(fā)燒時(shí)不能用于擦拭身體物理降溫,一般要用水把濃度降到30%左右,75%和30%的酒精的區(qū)別是100ml酒精中所含乙醇的量不同。
思考:請(qǐng)同學(xué)們觀察以下三個(gè)小燒杯里的硫酸銅溶液,看看有什么不同?
通過(guò)觀察可以直觀看到三個(gè)小燒杯里硫酸銅溶液的顏色不同,導(dǎo)致顏色不同的原因是濃度不同。
展示:生活中常見的用品。
觀察生活中常見的用品的標(biāo)簽,思考溶液濃度的表示信息。
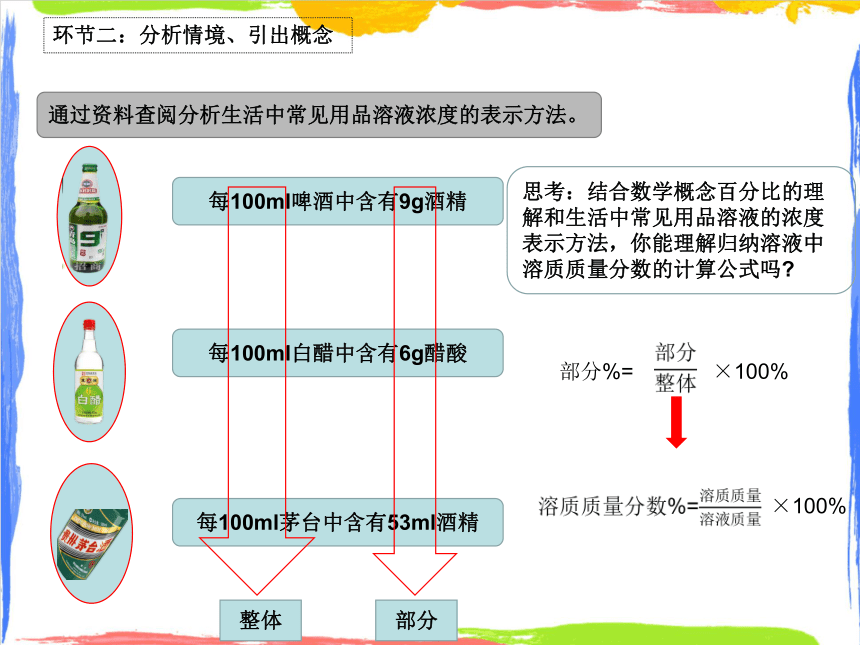
環(huán)節(jié)二:分析情境、引出概念
通過(guò)資料查閱分析生活中常見用品溶液濃度的表示方法。
每100ml啤酒中含有9g酒精
每100ml白醋中含有6g醋酸
每100ml茅臺(tái)中含有53ml酒精
整體
部分
思考:結(jié)合數(shù)學(xué)概念百分比的理解和生活中常見用品溶液的濃度表示方法,你能理解歸納溶液中溶質(zhì)質(zhì)量分?jǐn)?shù)的計(jì)算公式嗎
部分%=
×100%
溶質(zhì)質(zhì)量分?jǐn)?shù)%=
×100%
環(huán)節(jié)三:應(yīng)用概念、例題講解
例1:對(duì)溶質(zhì)的質(zhì)量分?jǐn)?shù)為15%的KCl溶液的含義理解錯(cuò)誤的是()
A.100gKCl溶液中溶解了15KgKCl
B.85g水中溶解了15KgKCl
C.100g水中溶解了15gKCl
D.KCl和水的質(zhì)量比為3:17
分析:結(jié)合溶質(zhì)質(zhì)量分?jǐn)?shù)的計(jì)算公式:
所以15%的KCl溶液中含有15g的KCl和95g的水,溶液總重量為100g.
錯(cuò)誤答案是C.
溶質(zhì)質(zhì)量分?jǐn)?shù)%=
×100%
15%的KCl溶液中15%=
×100%=
×100%
例2:計(jì)算以下三杯硫酸銅溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)。
1
2
3
0.1 g 無(wú)水硫酸銅
0.5 g 無(wú)水硫酸銅
2 g 無(wú)水硫酸銅
燒杯標(biāo)號(hào) 溶質(zhì)質(zhì)量 溶劑質(zhì)量 溶液質(zhì)量 溶質(zhì)的質(zhì)量分?jǐn)?shù) 備注
×100%
0.1g
20g
20.1g
0.5%
1
2
0.5 g
20g
20.5g
2.4%
2g
20g
22g
9%
3
1.1ml水的質(zhì)量為1g.
2.溶液質(zhì)量=溶質(zhì)質(zhì)量+溶劑質(zhì)量。
3.溶質(zhì)的質(zhì)量分?jǐn)?shù)=
環(huán)節(jié)四:對(duì)比分析、區(qū)分概念
討論:已知20度時(shí),氯化鈉的溶解度時(shí)36g。有人說(shuō):“20度時(shí)氯化鈉飽和溶液中溶質(zhì)質(zhì)量分?jǐn)?shù)為36%。”這種說(shuō)法對(duì)嗎?為什么?
固體的溶解度表示在一定溫度下,某固態(tài)物質(zhì)在100g溶劑里達(dá)到飽和狀態(tài)使所溶解的質(zhì)量。
溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)是溶質(zhì)質(zhì)量與溶液質(zhì)量之比,而溶液質(zhì)量等于溶質(zhì)質(zhì)量+溶劑質(zhì)量
環(huán)節(jié)四:對(duì)比分析、區(qū)分概念
分析:結(jié)合溶解度和溶質(zhì)質(zhì)量分?jǐn)?shù)的概念,分析對(duì)比20度時(shí),氯化鈉的溶解度是36g和溶質(zhì)質(zhì)量分?jǐn)?shù)為36%的氯化鈉溶液的區(qū)別。
20度時(shí)氯化鈉的溶解度是36g 溶質(zhì)質(zhì)量分?jǐn)?shù)為36%的氯化鈉溶液
溶質(zhì)質(zhì)量/g
溶劑質(zhì)量/g
溶液質(zhì)量/g
溶質(zhì)質(zhì)量分?jǐn)?shù)/%
通過(guò)對(duì)比分析可看出20度時(shí),氯化鈉的溶解度是36。有人說(shuō):“20度時(shí)氯化鈉飽和溶液中溶質(zhì)質(zhì)量分?jǐn)?shù)為36%。”這種說(shuō)法是不對(duì)的。溶解度和溶質(zhì)質(zhì)量分?jǐn)?shù)是兩個(gè)不同的概念。
36
100
136
26.5%
36
64
100
36%
環(huán)節(jié)四:對(duì)比分析、區(qū)分概念
一定溫度下,飽和溶液中溶質(zhì)質(zhì)量分?jǐn)?shù)和溶解度見的關(guān)系如下:
飽和溶液溶質(zhì)質(zhì)量分?jǐn)?shù)與溶解度之間的關(guān)系
飽和溶液溶質(zhì)質(zhì)量分?jǐn)?shù)= =
×100%
誤區(qū):常有同學(xué)直接用溶解度比100g求溶質(zhì)質(zhì)量分?jǐn)?shù)。
×100%
環(huán)節(jié)五:學(xué)以致用、回歸生活
學(xué)習(xí)了溶質(zhì)的質(zhì)量分?jǐn)?shù)后,我們就可以解決一些生活的計(jì)算問(wèn)題,如施用農(nóng)藥時(shí)可以準(zhǔn)確的計(jì)算一定量的藥業(yè)里所含農(nóng)藥的量;在工農(nóng)業(yè)生產(chǎn)中,可以通過(guò)計(jì)算確定選種用的氯化鈉和水的質(zhì)量,請(qǐng)同學(xué)們結(jié)合所學(xué)的內(nèi)容,完成以下練習(xí)。
練習(xí):在農(nóng)業(yè)生產(chǎn)上,常需要用質(zhì)量分?jǐn)?shù)為16%的氯化鈉溶液選種,現(xiàn)要配制150kg這種溶液,需要氯化鈉和水的質(zhì)量各是多少?
溶質(zhì)的質(zhì)量分?jǐn)?shù)%=
×100%
溶質(zhì)質(zhì)量=溶液質(zhì)量×溶質(zhì)質(zhì)量分?jǐn)?shù)
=150kg×16%
=24kg
溶劑質(zhì)量=溶液質(zhì)量-溶質(zhì)質(zhì)量
=150kg-24kg
=126kg
【練習(xí)3】某次蔗糖溶解實(shí)驗(yàn)過(guò)程如圖所示,不考慮水分蒸發(fā),下列判斷錯(cuò)誤的是( )
A.②中溶液是飽和溶液
B.③中溶液一定是不飽和溶液
C.②③中溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)不相同
D.③中溶液的溶質(zhì)質(zhì)量大于②中溶液的溶質(zhì)質(zhì)量
B
課后活動(dòng):
以小組為單位討論如果要配制50g質(zhì)量分?jǐn)?shù)為6%的氯化鈉溶液,同學(xué)們分析一下實(shí)驗(yàn)步驟核和實(shí)驗(yàn)注意事項(xiàng)有哪些?
展開更多......
收起↑
 資源預(yù)覽
資源預(yù)覽